
Efficiëntere geneesmiddelenontwikkeling met hulp van computermodellen
Het coronavirus heeft de wereld in zijn greep. Het vinden van een medicijn is nog nooit zo belangrijk geweest. Helaas zijn de ontwikkeling van nieuwe medicijnen en de ontwikkeling van een vaccin complexe, langdurige en vooral kostbare processen. Computermodellen kunnen dit proces versnellen. Wetenschappers van het Center for Computational Life Sciences (CCLS) onderzoeken deze modellen om de kosten van medicijnontwikkeling te verlagen en het proces te versnellen.
Traditioneel onderzoek is duur
‘De ontwikkeling van een geneesmiddel duurt gemiddeld meer dan tien jaar en kost meer dan een miljard dollar’, zegt Gerard van Westen, een van de onderzoekers verbonden aan CCLS. Hij werkt aan machine learning toegepast op de medicinale chemie om de chemische ruimte van potentiële nieuwe medicijnen te verkennen. ‘Een medicijn is een molecuul dat aan veel eisen moet voldoen. Aan de ene kant moet het zich houden aan het doelwit in het lichaam en aan de andere kant mag het geen bijwerkingen veroorzaken. Het moet ook de juiste eigenschappen hebben zodat het oplosbaar is; het moet worden geabsorbeerd in het lichaam en op de juiste plaats in het lichaam terecht komen. In mijn onderzoek moeten we al deze, vaak tegenstrijdige, doelen tegelijkertijd in evenwicht brengen.’
Als gevolg daarvan bereiken veel kandidaat-geneesmiddelen de eindstreep niet. Potentiële nieuwe geneesmiddelen worden vaak afgeschreven in de laatste fase waarin de medicijnen klinisch worden getest door vrijwilligers en patiënten. Met machine learning, of meer specifiek deep learning, worden nieuwe potentiële kandidaat-geneesmiddelen gegenereerd. Van Westen selecteert vervolgens met behulp van machine learning methodes de meest veelbelovende potentiële medicijnen. De medicijnen die de eindstreep waarschijnlijk niet halen, kan hij hiermee in een vroeg stadium afschrijven. Na selectie van de moleculen worden ze in het scheikunde lab geproduceerd en getest in biochemische testen, om te kijken of de moleculen zich gedragen zoals de computer voorspelde. ‘De betrokkenheid van computers maakt het hele proces efficiënter en kan kosten besparen', legt Van Westen uit.
Passende sleutel op het slot
‘Het molecuul moet in de receptor op het celmembraan passen. We zoeken dus eigenlijk in een stapel sleutels naar die ene sleutel die op het slot past', zegt Michael Emmerich, die ook verbonden is met CCLS. ‘In data zoeken we daarnaar met behulp van simulatie, oftewel 3-dimensional fitting. Het voordeel hiervan is dat uit de data alleen moleculen die zich daadwerkelijk kunnen binden aan de receptor worden geïdentificeerd als mogelijke kandidaten. Dit is echter inefficiënt, omdat elk molecuul apart moet worden onderzocht.' Volgens Emmerich is de oplossing machine learning in combinatie met multicriteria-optimalisatiealgoritmen. De multicriteria-optimalisatiealgoritmen maken het mogelijk om verschillende alternatieven of scenario's aan de hand van vele, vaak tegenstrijdige criteria te vergelijken. ‘Op basis van eerdere gegevens kunnen we voorspellen hoe een molecuul zich zal gedragen en of het zich uiteindelijk zal kunnen binden aan de receptor. Binnen het Leiden Institute of Advanced Computer Science (LIACS) doen we uitgebreid onderzoek naar deze machine leermodellen en koppelen ze aan multicriteria optimalisatiemethoden die de chemische ruimte van alle mogelijke moleculen kunnen doorzoeken.’
Detecteren van bijwerkingen
Zodra er een potentieel medicijn is gevonden kan High Throughput Screening (HTS) een uitkomst bieden om mogelijke bijwerkingen in kaart te brengen. HTS kan snel actieve verbindingen, antilichamen of genen identificeren, waarvan de resultaten aanknopingspunten bieden voor het ontwerp van geneesmiddelen en een inzicht in de interactie of de rol van geïdentificeerde biochemische processen. Lu Cao, universitair docent bij het LIACS en tevens verbonden aan CCLS, is expert op dit gebied. ‘Computer modellen kunnen een groot deel van de kandidaat-medicijnen filteren op basis van voorspellingen. Maar voorspellen hoe een medicijn daadwerkelijk reageert in een levend organisme is moelijker. HTS kan inzicht hierin geven doordat er wordt gewerkt met levende cellen. Eventuele bijwerkingen van een potentieel giftig geneesmiddel kunnen hierdoor voor het klinisch testen al ontdekt worden waardoor zo’n potentieel medicijn eerder afvalt.’
Coronavirus
In het kader van het coronavirus proberen de CCLS-onderzoekers te ondersteunen waar ze kunnen. Zo zoekt Emmerich met promovendus Patrick Echtenbruck en hoogleraar Boris Naujoks van de Technische Hochschule Keulen naar veelbelovende antivirale moleculen die al zijn goedgekeurd als geneesmiddel. Dit proces staat bekend als drug repurposing. Een idee is om een receptor van longcellen te binden, zoals de ACE2-receptor. Deze receptor is de plaats waar het SARS-CoV2-virus de cel binnenkomt en de replicatie begint. Emmerich ontwikkelde met zijn team en mensen van LACDR een machine learning programma om te bepalen of een molecuul geschikt is of niet met betrekking tot meerdere criteria. In een eerdere studie in samenwerking met Van Westen en LACDR bleek deze methode zeer succesvol voor andere soorten geneesmiddelen.
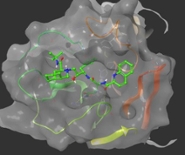
Van Westen lanceerde een driedimensionale virtuele screeningscampagne ('docking'), op zoek naar kleine moleculen die actief zijn tegen SARS-CoV-2-infectie. In een vergelijkbare repurposing aanpak omvatten de moleculen in de screening alle goedgekeurde geneesmiddelen die affiniteit hebben met bekende virale doelwitten zoals de virale protease. Ze hebben enkele potentieel actieve moleculen gevonden voor een follow-up screening en biologische validatie.
Op korte termijn is Emmerich voorzichtig met de verwachting veel bij te dragen aan de ontwikkeling van geneesmiddelen en vaccins voor Covid-19. Farmaceutische bedrijven die gespecialiseerd zijn in antivirale geneesmiddelen en vaccins doen namelijk hetzelfde onderzoek in cellijnen of zelfs in klinische opzet. ‘Ons onderzoek kan verbeteringen opleveren op de middellange en lange termijn,' zegt Emmerich. ‘Zodra de eerste geneesmiddelen beschikbaar zijn, zal de zoektocht naar alternatieve geneesmiddelen worden voortgezet, dat wil zeggen geneesmiddelen met minder bijwerkingen, minder kostbaar, of toepasbaar op een breder scala van patiënten. Hier zal ons onderzoek naar de multicriteria-aanpak van de ontwikkeling van geneesmiddelen nuttig zijn.’
