Eindelijk begrijpen we hoe zuurstof aan platina reageert
Platina is een veelgebruikte katalysator, maar de precieze werking ervan is voor wetenschappers grotendeels een mysterie. Ludo Juurlink heeft voor het eerst aangetoond hoe zuurstof reageert aan het platina-oppervlak. De bevindingen publiceert hij met de promovendi Kun Cao en Richard van Lent en internationale collega’s in het toonaangevende blad PNAS.
Juurlink scoort weer
Eerder dit jaar wist Juurlink samen met Richard van Lent en instituut DIFFER een veertig jaar oud probleem in de scheikunde op te lossen. Met behulp van een uniek gekromd platina-oppervlak – waar Juurlinks lab internationaal bekend om is – bewees hij op welke manier waterstof aan platina reageert. Bij het huidig onderzoek gebruikte hij wederom het gekromde platina, dit keer om de reactie met zuurstof te onderzoeken.
Hoe reageert zuurstof?
En dat leidde tot een interessante ontdekking. Juurlink ontdekte namelijk dat zuurstof op een andere manier reageert aan platina dan het veel lichtere waterstof. Voor deze ontdekking was het gekromde platina weer cruciaal. ‘Doordat het platinaoppervlak gekromd is, verloopt de atomaire structuur heel geleidelijk langs het oppervlak’, legt Juurlink uit. ‘Je kunt die structuur vergelijken met een trap, waarvan de treden naar de randen toe steeds smaller worden. In het midden lijkt het oppervlak meer op een balzaal.’ De reactiviteit van waterstof bleek af bleek te hangen van hoe dicht die traptreden van de katalysator op elkaar zitten. Bij zuurstof is dit ook het geval, maar om een fundamenteel andere reden. ‘De treden hebben een ander effect op zuurstof dan op waterstof.’
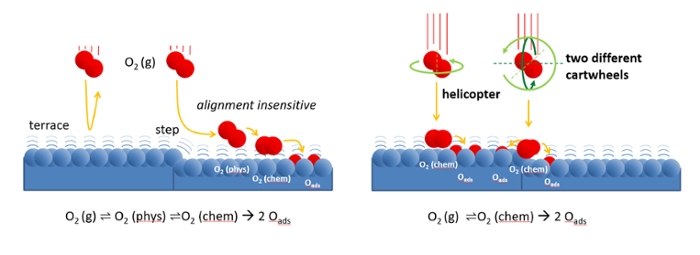
Figuur links: Zuurstofmoleculen benaderen met lage snelheid het katalysatoroppervlak. Hierbij verstrooien de treden van het oppervlak de moleculen tot een zwak gebonden staat, in het Engels: physisorbed. Van daaruit kan het molecuul gemakkelijk zijn weg vinden naar een plaats waar het chemisch bindt en uiteindelijk uiteenvalt. Op de atomair vlakke terrassen is de kans op verstrooiing in de gasfase veel groter.
Omdat de physisorbed toestand zwak gebonden is, lijkt deze sterk op het molecuul in de gasfase. In beide toestanden kan het molecuul draaien. Het verstrooiingsproces is daarom niet afhankelijk van de initiële oriëntatie van het molecuul.
Figuur rechts: Bij hoge invalsnelheid kunnen zuurstofmoleculen direct adsorberen in een chemisch gebonden toestand. Gekeken is naar moleculen die op twee manieren bewegen: helicoptering - draaien in een vlak dat parallel aan het oppervlak ligt - en cartwheeling - draaien in een vlak dat haaks op het oppervlak staat. Op terrassen hebben moleculen die 'helikopteren' een hogere kans om te binden. Alleen bij de randen van de treden maakt de richting waarin de cartwheeling moleculen draaien verschil. Moleculen die langs de rand van de treden roteren (donkergroene rotatie) blijven gemakkelijker aan de rand kleven dan de moleculen die roteren tegen de rand (lichtgroene rotatie).
Uniek lab in Japan
Volgens Juurlink heeft dat onder andere met de grotere massa van zuurstof te maken. ‘Doordat zuurstof zwaarder is dan waterstof, begint de interactie met het platina-oppervlak al op een grotere afstand,’ zegt hij. ‘Het zuurstofmolecuul voelt dan wel de interactie met platina, maar kan nog geen details waarnemen. Daardoor verloopt de reactie op een andere manier dan bij waterstof.’ Voor het experiment was het noodzakelijk de draaiingsrichting van de zuurstofmoleculen te kunnen sturen. Daar was een samenwerking met een Japanse collega voor nodig – Mitsunori Kurahashi – die daarvoor een uniek apparaat heeft gebouwd. ‘Ik heb vorig jaar zelf twee weken in zijn lab metingen mogen verrichten op een subsidie van het instituut waar Kurahashi werkt’, aldus Juurlink.
Waarom is deze ontdekking belangrijk?
Een mooie fundamentele ontdekking dus, concludeert Juurlink, die mogelijk ook invloed kan hebben op bestaande toepassingen. De reactie van zuurstof aan platina is namelijk essentieel in de duurzame energiesector en bij het verbeteren van de luchtkwaliteit. ‘Zo vindt de reactie plaats in waterstofbrandstofcellen en in uitlaatsystemen van auto’s,’ zegt de chemicus. ‘Dat wij nu op zo'n gedetailleerd niveau kunnen meten hoe de reactie verloopt, biedt uitdagingen aan theoretische modellen die deze chemische reactie beschrijven en er voorspellingen over doen.’
Lees het artikel in PNAS: Steps on Pt stereodynamically filter sticking of O2
