
Specifiek eiwit in de hoofdrol bij ziekte van Parkinson
Met elektronspins hebben natuurkundigen het bindingsproces onderzocht van het eiwit α-synucleïne, dat wordt geassocieerd met de ziekte van Parkinson. Wat blijkt is dat het eiwit op een verrassend efficiënte manier bindt aan een hersenmembraan. Met deze in Leiden ontwikkelde methode hebben de onderzoekers de hoofdrol van het eiwit bevestigd bij het overdragen van signalen tussen zenuwcellen in de hersen. Publicatie in PLoS ONE.
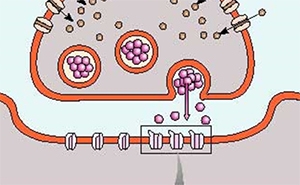
Ziekte van Parkinson
De ziekte van Parkinson is de op een-na-meest voorkomende neurodegeneratieve aandoening ter wereld. In de hersenen van een Parkinsonpatiënt gaat er iets mis met het transport van neurotransmitters, die de communicatie binnen het brein verzorgen. Maar wat er nu precies misgaat is nog onbekend. Wetenschappers hebben wel al ontdekt dat eiwitten zich ophopen in de hersenen, en α-synucleïne komt daar opvallend vaak voor. De verdachte dominante aanwezigheid van dit eiwit was voor groepsleider dr. Martina Huber aanleiding voor een onderzoek naar zijn gedrag.
Traceertechniek
Haar groep bestudeerde de binding van α-synucleïne aan blaasjes (vesikels) met hun traceertechniek electron paramagnetische resonantie (EPR). Ze plaatsten op verschillende plekken labels op het molecuul, en door hun elektronspins te manipuleren, konden ze steeds bijhouden waar de labels zich bevonden. Zo hielden ze in de gaten wat het eiwit allemaal in zijn schild voert. Ze maten de bewegelijkheid van de labels om te bepalen welke plekken van het eiwit het sterkst binden, en dus het minste bewegen.
Verrassing
‘Tot mijn verbazing bleek α-synucleïne verrassend goed te binden,’ zegt Huber. ‘Dit soort blaasjes heeft normaal gesproken een slechte binding omdat het niet heel negatief is geladen. Maar toch zien we nu dit resultaat.’ Die uitkomst levert een stukje van de complexe puzzel rond de oorzaak van Parkinson.
Artikel
Parkinson’s Protein α-Synuclein Binds Efficiently and with a Novel Conformation to Two Natural Membrane Mimics, Pravin Kumar, Ine M. J. Segers-Nolten, Nathalie Schilderink, Vinod Subramaniam, Martina Huber
Huber: ‘Bij een ziekte spelen er meestal veel processen, waaronder de echte malafide processen, maar ook lichaamseigen correctiemechanismen die hun werk goed doen of juist falen. We moeten al die puzzelstukjes in kaart brengen om te zien waar het precies fout gaat. We zien nu dat α-synucleïne in elk geval een belangrijke rol speelt bij Parkinson. Je hebt veel meer kans om een behandeling te vinden als je snapt hoe een ziekte werkt, dus het is belangrijk dat we daar een stapje dichter bij zijn.’
