
De moleculaire achtergrond van hydrofiel/hydrofoob gedrag
Onderzoekers van het Leiden Institute of Chemistry hebben aangetoond dat ook minimale verschillen in structuur van oppervlaktes hydrofoob gedrag kunnen bepalen. Hun onderzoek werd op 30 september gepubliceerd in het toonaangevende blad ‘Physical Reviews Letters’.

Iedereen kan met eigen ogen zien dat watermoleculen elkaar aantrekken. Als watermoleculen een sterkere interactie met elkaar hebben dan met het oppervlak waar ze op liggen, dan vormt het een druppel. Een Tefal pan en het blad van de lotus plant zijn voorbeelden van dergelijke hydrofobe oppervlakken, waar water liever weinig mee te maken heeft. Onderzoek naar water in koolstofnanobuisjes had al aangetoond dat niet alleen de interactie tussen moleculen onderling en met het oppervlak relevant is, maar ook de grootte van het volume en de temperatuur.
Atomaire schaal
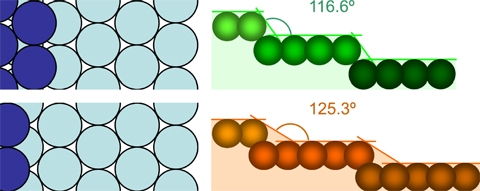
Onderzoekers aan het Leiden Institute of Chemistry (MJTC van der Niet, A. den Dunnen, Marc Koper, Ludo Juurlink) hebben nu aangetoond dat ook minimale verschillen in de structuur van het oppervlak doorslaggevend kunnen zijn. In een artikel in het toonaangevende blad Physical Review Letters laten dr. Janneke van der Niet en haar collega’s zien dat twee bijna identieke schone, gestapte oppervlakken van het platina hydrofiel zijn. De oppervlakken zien er op atomaire schaal uit als een trap waarvan de trede ongeveer 3x breder is dan het hoogteverschil tussen de treden. Het enige verschil tussen de twee oppervlakken is de ordening van de atomen die de staprand vormen. De experimenten laten zien dat water sterker bindt aan stapranden dan op de terrassen, maar dat beide gestapte oppervlakken hydrofiel zijn. Water bedekt het hele oppervlak middels een monolaag van H2O moleculen voordat een tweede waterlaag zich vormt.
Verrassing voor onderzoekers
Het verrastte de onderzoekers dat slechts één van de twee gestapte oppervlakken hydrofoob wordt wanneer de oppervlakken eerst met deuterium (D) atomen (een isotoop van waterstof H) worden bedekt. De andere blijft hydrofiel. De manier waarop het water van het oppervlak verdampt en de hoeveelheid chemische interactie die het water heeft gehad met het oppervlak geven dit verschil aan. De chemische interactie wordt op slimme manier bepaald door de uitwisseling van D en H atomen tussen watermoleculen en het oppervlak te meten. Ook laten de experimenten zien dat één enkele monolaag van watermoleculen al in staat is de vorming van het gas D2 aan het oppervlak tegen te houden.
Watermoleculen ordenen
Van der Niet en collega’s denken dat het verschil in het hydrofobe of hydrofiele gedrag van het oppervlak te herleiden is tot de manier waarop de eerste watermoleculen zich aan de stapranden ordenen. Deze ordening bepaalt waarschijnlijk of extra watermoleculen zich liever in een 2-dimensionaal netwerk over het hele oppervlak uitspreiden of dat ze liever zich opstapelen langs de stapranden. Klaarblijkelijk maakt het deuterium dat tussen het water en het platina zit het kleine, cruciale verschil waardoor deze oppervlakken zich tegengesteld gaan gedragen. De auteurs geven aan dat dit wellicht te maken heeft met verschillen in de bindingssterkte van het deuterium met de stapranden.
Links
Het wetenschappelijk artikel in Physical Review
