
Schone energie uit zeewater een stap dichterbij
De onderzoeksgroep van Leids chemicus Marc Koper heeft een katalysator ontdekt die de productie van chloorgas tijdens de elektrolyse van zout water minimaliseert. De uitvinding kan de directe productie van waterstof uit zeewater mogelijk maken. Het artikel is gepubliceerd in de Journal of the American Chemical Society.
Chloorgas en zuurstof
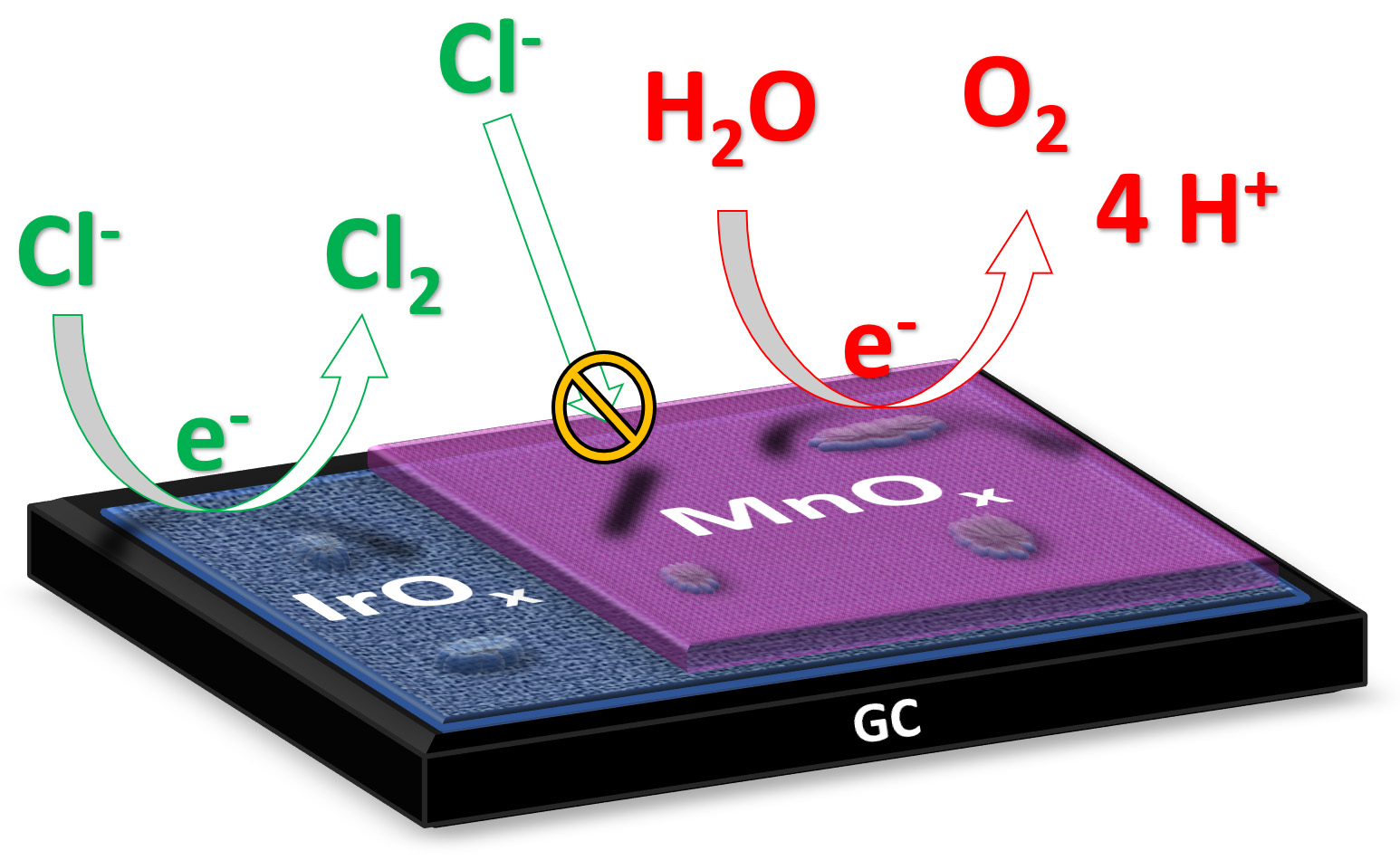
‘Bij de elektrolyse van zout water, zoals zeewater, is het uiteindelijke doel om waterstof te produceren aan de kathode,’ legt promovendus Jan Vos van het Leids Instituut voor Chemie uit. ‘Het gevormde product aan de anode is idealiter zuurstof, omdat dit onschadelijk is voor het milieu.’ Bij de elektrolyse van zout water kan echter tegelijkertijd ook giftig chloorgas aan de anode ontstaan. De onderzoekers hebben nu een katalysator geproduceerd die de vorming van chloorgas minimaliseert ten faveure van de zuurstofvorming. Vos legt uit: ‘De katalysator bestaat uit twee metaaloxides: iridium oxide met daarop een laagje mangaan oxide van slechts een tiental nanometers dik. Iridium is een materiaal dat hoge katalytische activiteit vertoont voor de vorming van zowel zuurstofgas en chloorgas; het mangaanoxide werkt als een soort membraan dat de aanvoer van chloride ionen verhindert en de vorming van chloorgas onderdrukt.’
Elektrolyse
Bij elektrolyse van water stuurt men stroom door het water om het te splitsen in andere stoffen. In de gewenste reactie splitst vloeibaar water (H2O) in zuurstofgas (O2) en waterstofgas (H2). In zout water is natriumchloride (NaCl) aanwezig als opgeloste natrium- en chloorionen (Na+ en Cl-). In dit geval kan er tijdens de elektrolyse ook een tweede reactie optreden, waarbij de chloorionen worden omgezet in chloorgas (Cl2).
Schone energie
Volgens Vos is de elektrolyse van water een belangrijke stap voor de productie en het gebruik van waterstof als alternatieve energiedrager. Een anode die de vorming van chloorgas tegengaat, maakt waterelektrolyse mogelijk waarbij het niet nodig is het gebruikte water eerst te ontdoen van opgelost zout. Dit kost nu nog erg veel energie en kapitaal. Het zou de directe productie van waterstof uit zeewater mogelijk maken, en zo de zeldzame zoetwaterreserves op aarde ontlasten.
Een nuttige bijwerking van de elektrolyse van zout water is volgens Vos de productie van zeer zuiver zoet water. ‘Als het gewonnen waterstofgas uiteindelijk wordt gebruikt als brandstof, bijvoorbeeld in een brandstofcel in een auto, reageert de waterstof met zuurstofgas uit de atmosfeer weer terug tot water. De grootschalige toepassing van waterelektrolyse en waterstof in brandstofcellen zal leiden tot grote hoeveelheden van dit 'zuivere afvalwater'; in een toekomst waar watertekorten een steeds nijpender probleem worden zou dit zeker niet onwenselijk zijn.’
Chloor-blokkade
Het onderzoek werpt nieuw licht op een vraagstuk in de chemie dat al tientallen jaren speelt. ‘Oorspronkelijk hadden we geen idee waarom materialen gebaseerd op mangaanoxide zo'n hoge selectiviteit jegens zuurstof hadden. We gingen ervan uit dat het puur een katalytische eigenschap van het materiaal was, maar mogelijke effecten van diffusiebarrières: het selectief blokkeren van het transport van chloride ionen... Dat kwam niet eens in ons op! In feite is het een heel basale, effectieve oplossing voor een zeer complex probleem. Dat heeft onze onderzoeksrichting radicaal veranderd.’
Selectiviteit
De ontdekking heeft implicaties voor selectiviteit in elektrolyse. Selectiviteit is een belangrijk criterium voor hoe goed een katalysator werkt. Bij veel (elektro)chemische processen is het namelijk mogelijk om verschillende producten te vormen tijdens een reactie, en men wil dat alleen het gewenste product wordt gevormd. De manier om selectiviteit te beïnvloeden, is doorgaans om de katalysator heel precies te kiezen en nauwkeurig 'af te stellen', maar dit kost veel tijd en geld. Bovendien is het hierbij niet altijd mogelijk om hoge selectiviteit te combineren met hoge activiteit, een andere belangrijke eigenschap.
Volgens Vos past het onderzoek mooi in een opkomende, alternatieve trend binnen elektrokatalyse: het gebruikt van bepaalde coatings om een katalysator te verbeteren. ‘Zo'n laagje verhindert dat ongewenste reactanten de katalysator kunnen bereiken. Hiermee kan een actief maar aselectief katalytisch materiaal op een alternatieve manier selectief gemaakt worden.’
Bron
Vos, J.G.; Wezendonk, T.A.; Jeremiasse, A.W. en Koper, M.T.M., 2018. MnOx/IrOx as Selective Oxygen Evolution Electrocatalyst in Acidic Chloride Solution. J. Am. Chem. Soc. , article ASAP. DOI: 10.1021/jacs.8b05382
