
Katalyse in nieuw licht
Katalysatoren, zoals die in de auto, bestaan vaak uit piepkleine metaalbolletjes. Op hun oppervlak verlopen de chemische reacties extra snel. Een katalysator zorgt ervoor dat de chemische reactie tussen twee stoffen sneller of beter verloopt. Katalysatoren zijn onmisbaar in de chemische industrie. De autokatalysator zorgt er onder andere voor dat het giftige koolmonoxide wordt omgezet in het onschadelijke kooldioxide.
Realistische omstandigheden
Katalyse vindt meestal plaats bij hoge gasdrukken. Toch is onze kennis over de reactieprocessen voornamelijk afkomstig van nauwkeurig onderzoek in een vacuümomgeving. De onderzoekers in Leiden en Grenoble hebben ontdekt dat het katalysatoroppervlak bij realistische drukken een andere gedaante kan aannemen dan in vacuüm. In de buitenste atoomlagen vormen zich nieuwe structuren met nieuwe samenstellingen, bijvoorbeeld een oxidelaagje met een dikte van slechts één atoom. Ook al is de dikte van dit laagje nog zo bescheiden, de chemische reacties veranderen er volledig door. De onderzoekers zagen deze verandering bij de naverbranding van koolmonoxide op de metalen platina en palladium, een van de reacties in de autokatalysator. Geheel tegen de gangbare verwachtingen in blijkt het oxidehuidje de katalysator sterk te verbeteren.

Schakelaar
Een tweede ontdekking is dat het oppervlak van de katalysator soms spontaan heen en weer schakelt tussen de twee structuren, terwijl de katalysator daarbij afwisselend goed en slecht werkt. Nu komen chemische oscillaties wel vaker voor, maar meestal hebben deze geen abrupt karakter. Ze lijken meer op de populatievariaties in de welbekende prooi-roofdiercyclus. Het team uit Leiden en Grenoble moest dus op zoek naar de verborgen motor achter de oscillaties. En als het oppervlak kan schakelen, kan het dan ook in de meest efficiënte stand gehouden worden om zo de chemische processen nog verder te versnellen?
Vicieuze cirkel
De metingen laten zien dat verruwing en egalisatie van het oppervlak de motor achter de abrupte structuurwisselingen vormen. Wanneer de katalysator bedekt is met een dun oxidehuidje wordt het door de reactie gaandeweg ruwer. Dat komt omdat de koolmonoxidemoleculen telkens zuurstofatomen aan het laagje onttrekken, waarbij metaalatomen over het oppervlak worden verplaatst. Deze verruwing gaat door totdat het oxidehuidje niet langer de gunstigste structuur is. Op dat moment verandert het oppervlak plotseling van een oxide naar een metaal. De chemische reactie op het metaal veroorzaakt geen verdere verruwing. Integendeel, de metaalatomen kunnen zich dan vrij verplaatsen en ‘repareren’ het ruwe oppervlak dat daardoor juist steeds vlakker wordt. Totdat het zo vlak is, dat de oxidestructuur de gunstigste optie is. Het oppervlak schakelt dan plotseling terug naar de oxidevorm en het hele proces begint weer van voor af aan. In principe moet het mogelijk zijn om de ruwheid van het oppervlak tegen te gaan dan wel om de mobiliteit van de atomen van het oxide te laten toenemen. Dat zou het optimale werkingsgebied van de katalysator enorm verruimen.
Nieuwe microscopen
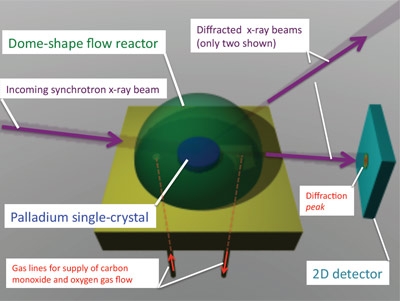
Het klinkt simpel, maar toch waren de beschreven waarnemingen eerder niet mogelijk. Het is moeilijk om onder de realistische omstandigheden van hoge temperaturen, hoge drukken en stromende gasmengsels de precieze atoomstructuur van oppervlakken in kaart te brengen. Hiervoor waren speciale, nieuwe instrumenten nodig. De onderzoekers in Leiden en Grenoble hebben daarom twee nieuwe apparaten ontwikkeld. Een Scanning Tunneling Microscoop (STM) met miniatuur reactorvat, waarin een vlijmscherp naaldje het katalysatoroppervlak aftast. En een reactor voor oppervlakteröntgendiffractie, waarin intense röntgenstraling het actieve oppervlak doorlicht. Met deze apparatuur kunnen ze het oppervlak tot atoomniveau bestuderen én tegelijkertijd de reactiesnelheid meten. Deze combinatie was tot nog toe niet mogelijk.
11 juli 2010/Universiteit Leiden en Technologiestichting STW
